Anvisa concluiu a certificação de Boas Práticas de Fabricação da Pfizer
Todas as empresas envolvidas no processo fabril e requisitadas pela Pfizer já estão devidamente certificadas quanto ao cumprimento das BPF.
equipe técnica da Anvisa concluiu a análise das informações enviadas pela Pfizer para a verificação do cumprimento das Boas Práticas de Fabricação (BPF) pelas três novas empresas incluídas em seu processo fabril, visando a obtenção do registro da vacina contra a Covid-19.
De acordo com a Pfizer, as seguintes empresas participam dos processos de fabricação do insumo farmacêutico ativo (IFA) biológico, bem como da formulação da sua vacina:
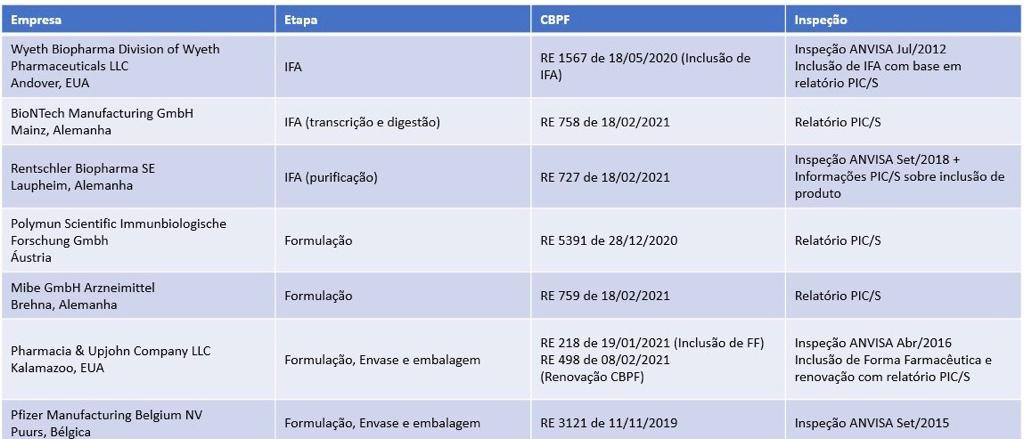
Com isso, todas as empresas envolvidas no processo fabril e requisitadas pela Pfizer já estão devidamente certificadas quanto ao cumprimento das BPF.
A Certificação de Boas Práticas de Fabricação é feita de forma individual para cada fábrica presente no processo. Todas as empresas envolvidas na produção de algum medicamento ou vacina precisam estar certificadas.
Duas formas de emitir a certificação
A verificação do cumprimento das boas práticas de fabricação de medicamentos durante a pandemia pode ser realizada por meio de dois diferentes mecanismos, conforme estabelecido pela Resolução RDC 346/2020, visando a agilidade, bem como a garantia da qualidade dos medicamentos. A primeira é a inspeção realizada pela Anvisa, quando servidores da Agência fazem a inspeção diretamente. A segunda é por meio de relatórios de inspeção elaborados por autoridades reguladoras com equivalência regulatória à agência brasileira. Essas autoridades, junto com a Anvisa, compõem o Esquema de Cooperação de Inspeção Farmacêutica (PIC/S, em sua sigla em inglês).
No caso da vacina da Pfizer/BioNTech, a verificação do cumprimento das BPF das empresas que participam do processo de fabricação da vacina foi realizada por meio desses dois mecanismos: quatro empresas tinham inspeção anterior realizada diretamente pela Anvisa e três foram inspecionadas por autoridade reguladora equivalente, sendo certificadas por meio de relatórios emitidos por autoridades participantes do PIC/S. Além disso, informações provenientes dessas autoridades foram utilizadas para avaliação da inclusão desse novo produto na linha de produção.
PIC/S
Em 1º de janeiro de 2021, a Anvisa se tornou o 54º membro do PIC/S, passando a contar com o reconhecimento internacional da excelência das inspeções em Boas Práticas de Fabricação (BPF) de medicamentos e insumos farmacêuticos de uso humano. Esta iniciativa internacional em inspeção farmacêutica está voltada para duas principais atividades:
- Harmonização internacional, por meio do estabelecimento de guias de referência na área de Boas Práticas de Fabricação e de Distribuição de produtos farmacêuticos.
- Realização de treinamentos a fim de tornar equivalentes os sistemas de inspeção de boas práticas de fabricação de todo o mundo.